ABO血型系统作为人类免疫系统的重要组成部分,其抗原分子直接影响机体对病原体的识别与防御能力。研究表明,A型血人群的红细胞表面携带A抗原,血清中则存在抗B抗体,这种独特的分子结构可能使其在感染特定病毒时面临更高风险。例如,新冠疫情初期,武汉多家医院及欧洲研究机构发现,A型血患者感染后出现呼吸衰竭的比例显著高于其他血型,而O型血人群感染率和重症率均较低。这一现象在SARS疫情中亦有体现,O型血医护人员感染率仅为42.1%,远低于非O型血的88.5%。
进一步研究发现,ABO血型基因座(9q34.2)与新冠病毒诱导的呼吸衰竭存在关联。A型血患者体内某些免疫细胞(如单核细胞)的过度活跃可能导致炎症介质释放增加,加剧血管内皮损伤。美国23andMe平台对75万人的调查显示,O型血感染风险低9%~18%,而A型血人群的免疫应答可能更易触发“细胞因子风暴”。这些发现揭示了血型与免疫防御机制的深层联系,但学者也强调,病毒变异和个体差异可能削弱此类关联的普适性。
二、心血管疾病与血栓形成的高危倾向
A型血人群的血液特性使其在心血管疾病领域备受关注。2024年美国一项覆盖60万人的研究发现,A型血人群在60岁前发生缺血性中风的风险比其他血型高16%,早发中风患者中A型血占比高达48%。这一现象可能与A型血人群体内von Willebrand因子水平较高有关,该蛋白促进血小板凝聚,增加血栓形成风险。上海交通大学长达25年的队列研究进一步证实,A型血人群患胃癌和结直肠癌的风险分别比非A型血高18%和12%,而消化道肿瘤与慢性炎症及血管异常增生密切相关。
值得注意的是,AB型血虽未直接被称为“危险血型”,但其血栓风险在所有血型中最高。非O型血人群发生下肢深静脉血栓和肺栓塞的风险是O型血的1.75-1.92倍。这种差异源于ABO抗原对凝血因子Ⅷ和血管性血友病因子的调控作用,提示血型可能成为个性化抗凝治疗的潜在参考指标。
三、癌症易感性的遗传密码
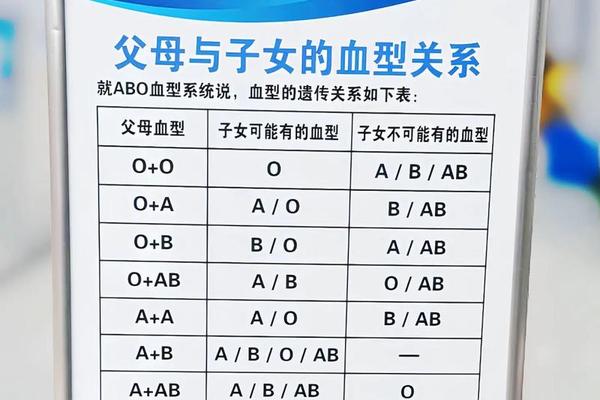
血型与癌症的关联性在多项大规模研究中得到验证。A型血人群的消化道肿瘤风险尤为突出:与O型血相比,其胃癌发病率增加25%,癌风险升高23%。分子机制研究表明,A抗原可能通过改变肠道微生物群构成或增强致癌病原体(如幽门螺杆菌)的黏附能力,促进慢性炎症向癌变转化。而AB型血人群则表现出独特的肝癌易感性,患病风险比A型血高45%。
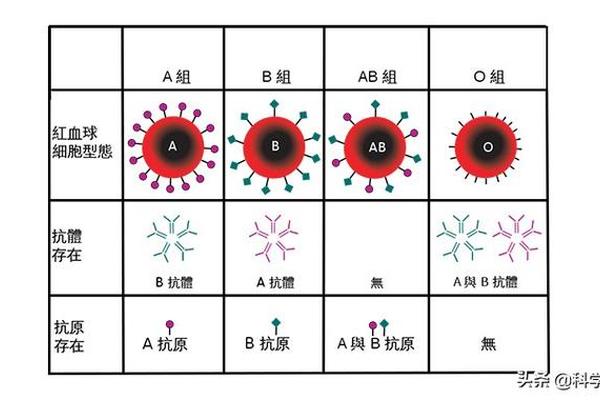
这种差异不仅限于实体肿瘤。瑞典卡罗琳斯卡医学院发现,A型血与49种疾病显著相关,包括白血病和淋巴瘤。上海交通大学团队推测,ABO基因可能通过调控细胞表面糖基化修饰,影响肿瘤微环境中免疫细胞的识别与清除功能。尽管如此,B型血人群在多数癌症中的低风险提示,血型并非决定癌症命运的单一因素。
四、生殖健康与妊娠并发症的潜在影响
血型对女性生殖健康的影响在近年逐渐显现。研究表明,A型血孕妇发生子痫前期的风险较O型血增加15%,而AB型血孕妇的妊娠相关静脉血栓栓塞症(PA-VTE)发病率是非AB型血的1.4倍。这种风险差异可能与血型特异性凝血因子水平有关:A型血孕妇的纤维蛋白原浓度普遍偏高,导致胎盘血流灌注异常。
对于AB型血男性,其细胞表面抗原的免疫原性可能引发配偶生殖道局部免疫反应。临床数据显示,AB型血男性配偶的复发性流产发生率较其他血型高8%,但具体机制仍需进一步验证。这些发现为辅助生殖技术中的免疫干预提供了新思路,例如针对血型抗原的抗体筛查和免疫调节治疗。
五、争议与个体差异的复杂性
尽管大量研究支持血型与疾病风险的相关性,学界仍存在争议。哥伦比亚大学对7770名新冠患者的分析显示,O型血的保护效应“微乎其微”,血型对临床决策的影响权重低于1%。马萨诸塞州综合医院的外科医生更直言,从未将血型纳入病情评估体系。这种分歧源于研究方法的局限性:多数结论基于流行病学统计,缺乏直接的分子机制证据;样本的地域偏倚(如亚洲A型血占比达28%)也可能放大关联性。
个体差异的调节作用不容忽视。上海交通大学研究指出,A型血人群若保持健康生活方式,可降低40%的中风风险。遗传学家强调,ABO基因仅占疾病遗传风险的3%-5%,后天的环境暴露和表观遗传修饰才是核心变量。“危险血型”的标签更应被视为风险提示而非命运判决。
总结与展望
A型血被称为“危险血型”的背后,是ABO抗原系统与免疫、凝血、细胞信号传导等多重生理过程的复杂互动。从新冠肺炎重症风险到消化道肿瘤易感性,从妊娠并发症到心血管事件,血型如同一把双刃剑,既可能成为疾病预警的生物标志物,也可能因过度解读引发不必要的焦虑。未来研究需在三个方向突破:一是建立跨种族、跨地域的超大规模队列,消除样本偏倚;二是解析ABO基因与其他遗传位点的交互作用;三是开发基于血型的个性化预防策略,例如针对A型血人群的早期癌症筛查方案或定制化抗凝治疗。正如浙江医院专家所言,血型研究的意义不在于制造恐慌,而在于为健康管理提供更精细的导航。


