在人类血型系统中,ABO和Rh血型不合是新生儿溶血病的主要诱因。当父母血型存在特定组合时,胎儿可能遗传与母亲相异的血型抗原,引发母体免疫系统产生抗体攻击胎儿红细胞。以父母一方为AB型、孩子为A型的组合为例,若母亲为O型血、父亲为AB型血,胎儿有50%概率为A型或B型,此时母体产生的抗A/B抗体会通过胎盘引发溶血反应。这种免疫冲突虽不常见,却可能对新生儿健康造成威胁,需要科学认知与规范管理。
血型遗传与溶血机制
血型遗传遵循孟德尔定律,AB型血父母携带A和B显性抗原基因,当与A型血配偶结合时,孩子可能继承A型或AB型血型。根据上海第一妇婴保健院严虎医生的研究,O型血母亲体内天然存在的抗A/B抗体(IgG型)能穿透胎盘屏障,与胎儿红细胞表面的A/B抗原结合,激活补体系统导致红细胞破裂。
溶血反应的核心在于"抗原-抗体复合物"的形成。ABO溶血中,胎儿红细胞表面的A/B抗原数量仅为成人的1/3,且母体抗体可被胎盘组织中的可溶性抗原部分中和,因此病情通常较轻。相比之下,Rh溶血因D抗原免疫原性更强,常导致更严重的贫血和胆红素脑病,但我国汉族人群Rh阴性率仅0.3%,临床发生率较低。
高风险血型组合分析
临床数据显示,母婴ABO血型不合发生率约15%-20%,但仅2%-2.5%发展为显性溶血病。高风险组合包括:
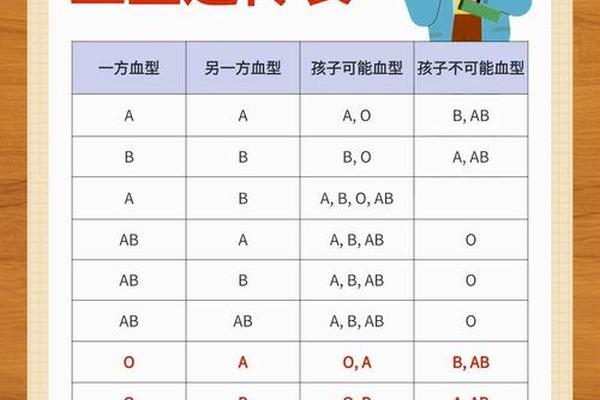
1. 母亲O型+父亲A/B/AB型:胎儿可能为A/B型,母体抗A/B效价超过1:64时风险显著上升。其中父亲为AB型时,胎儿100%为A/B型,理论风险最高。
2. 母亲Rh阴性+父亲Rh阳性:二胎发生Rh溶血的概率达50%-90%,首胎需通过抗D免疫球蛋白预防。
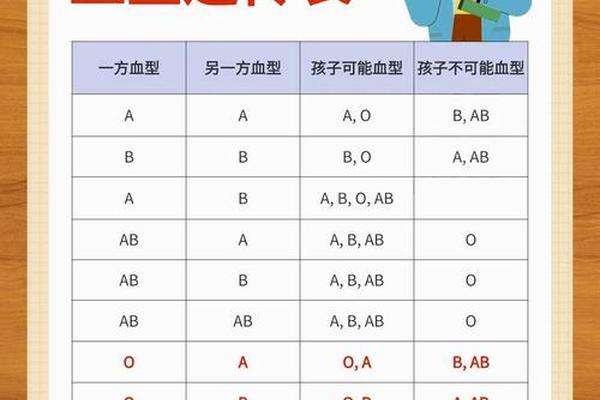
值得注意的是,A型血母亲与AB型父亲组合中,胎儿可能为A/AB型。由于A型母亲体内不含抗A抗体,此类组合不会引发溶血,这与O型血母亲的免疫机制存在本质差异。这解释了为何AB型父亲与不同血型母亲的溶血风险呈现显著差异。
临床诊断与干预策略
产前诊断体系包含三重防线:孕早期夫妻血型筛查、孕中期抗体效价监测、孕晚期脐血穿刺分析。中国人民解放军联勤保障部队第九00医院的研究表明,采用母体外周血胎儿游离DNA检测技术,可在孕12周无创判断胎儿Rh血型,准确率达99.3%。对于ABO溶血高风险孕妇,动态监测抗A/B效价变化,结合超声评估胎儿肝脾肿大程度,能有效预测疾病严重程度。
治疗层面形成阶梯化方案:光疗作为首选干预手段,可将未结合胆红素转化为水溶性异构体排出;丙种球蛋白通过阻断Fc受体抑制溶血进程;当血清总胆红素超过342μmol/L时,换血治疗可置换出85%致敏红细胞。北京清华长庚医院2022年临床数据显示,规范治疗下ABO溶血病治愈率达98.7%,仅0.3%重症病例遗留神经损伤。
预防体系与研究进展
预防策略呈现时空二维特性:孕前通过血型基因检测识别高危夫妇;孕期对Rh阴性母亲实施抗D免疫球蛋白被动免疫;产后新生儿即刻进行Coombs试验筛查。2022年《儿科输血指南》推荐,O型血孕妇在孕16周、28周分别检测抗体效价,结合基因芯片技术预测胎儿血型,将漏诊率降至1.2%。
当前研究聚焦于两大方向:一是开发重组抗D单克隆抗体替代血浆来源制剂,降低感染风险;二是探索CRISPR基因编辑技术修饰胎儿红细胞抗原表达。复旦大学附属儿科医院正在进行的"人造脐血"研究,试图通过体外培养干细胞获得通用型红细胞,为重度溶血患儿提供新型治疗选择。
母婴血型不合导致的溶血病是免疫遗传学与围产医学交叉的典型病症。现有证据表明,父母AB型与A型孩子的组合本身不构成溶血风险,真正危险源于O型血母亲与非O型血父亲的特定组合。通过完善三级预防体系,90%以上的溶血病可被早期识别和有效控制。未来随着表观遗传学和纳米生物技术的发展,有望实现胎盘屏障的靶向调控,从根本上阻断抗体传输路径。建议育龄夫妇孕前进行扩展血型筛查,医疗机构建立区域性溶血病监测网络,共同守护新生儿生命健康。


