在当代健康话题中,血型与疾病风险、饮食模式的关系始终备受关注。A型血作为全球人口中占比约30%的常见血型,近年来因多项研究揭示其与中风、心血管疾病及特定感染风险的关联,被冠以“危险血型”的标签。与此以“A型血饮食法”为代表的个性化营养理论,主张通过调整饮食结构来降低健康隐患。这种看似矛盾的现象——既被贴上风险标签,又存在针对性解决方案——引发了公众对血型科学价值的深度思考。本文将从饮食调整、疾病机制、科学争议三个维度,探讨A型血的健康特性及其应对策略。
一、饮食调整:植物性饮食的争议与价值
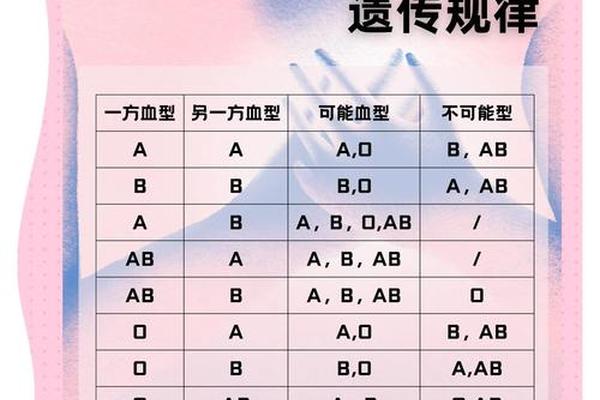
“A型血饮食法”最早由美国自然疗法医师彼得·德达莫提出,认为A型血源于农耕文明,其消化系统更适应以植物为主的膳食结构。具体建议包括:优先选择豆腐、深绿叶菜、鳕鱼等低脂高纤维食物,严格限制红肉、乳制品及加工食品的摄入。支持者指出,这类饮食模式通过降低胆固醇和血液黏稠度,可能缓解A型血人群的代谢负担。
加拿大研究团队在2024年的对照实验中发现,当不同血型人群统一采用偏素食的A型饮食时,心血管代谢指标(如甘油三酯、腰围)均呈现改善趋势,表明获益源于素食本身而非血型匹配。这揭示了“血型饮食法”的局限性:其效果可能更多来自饮食结构的优化,而非血型特异性机制。尽管如此,A型血人群仍需警惕高脂饮食的风险,因为其血液中天然存在的von Willebrand因子水平较高,更易形成血栓。
二、疾病风险:从凝血机制到免疫应答
多项流行病学研究证实,A型血人群的中风发病率比其他血型高出30%。究其根源,A型红细胞表面的A抗原不仅影响凝血功能,还与特定病原体的结合能力相关。例如,新冠病毒的刺突蛋白可通过模拟A抗原结构,更易入侵A型血个体的呼吸道细胞,导致感染后呼吸衰竭风险增加56%。这种分子层面的“钥匙-锁”机制,解释了为何A型血在新冠大流行中成为重点关注对象。
在凝血系统中,A型血人群的von Willebrand因子浓度比O型血高25%,这使得血小板更易聚集,形成动脉粥样硬化斑块。哈佛大学2023年的队列研究显示,A型血冠心病患者的血栓事件发生率是其他血型的1.4倍,尤其在合并高血压时风险倍增。而肠道微生物的最新研究揭示,A型血特有的糖基化修饰可能改变肠道菌群构成,通过“肠-脑轴”加剧炎症反应,进一步升高神经血管疾病风险。
三、科学争议:先天宿命论与后天干预论
尽管A型血的健康风险得到部分研究支持,学术界仍存在显著分歧。哥伦比亚大学团队对7770名新冠患者的分析显示,A型血感染率仅比O型血高3%,统计学差异微弱。反对者强调,将复杂疾病归因于单一血型因素过于简化,例如中风风险还受BMI、运动习惯等后天因素调控,A型血本身贡献度不足15%。
针对“危险血型”的标签,伦敦大学遗传学家Sarah Tishkoff提出新视角:A抗原在古代可能赋予抗疟疾优势,其健康代价是现代生活方式引发的“进化失配”。这提示风险并非不可逆转——通过低盐饮食、定期监测血压等措施,A型血人群可有效控制70%的中风诱因。2025年剑桥大学的血型转换技术突破更展现未来可能性:利用嗜黏蛋白阿克曼菌的酶制剂,可清除红细胞表面A抗原,使其具备O型血的兼容特性。
总结与展望
A型血与特定疾病的相关性,反映了基因与环境交互作用的复杂性。当前证据表明,其风险主要源于凝血机制活跃、免疫应答特性及病原体易感性,但通过植物性饮食、定期体检等干预手段,可显著降低健康威胁。未来研究需在两方面突破:一是利用全基因组关联分析,厘清血型基因与其他风险位点的协同效应;二是开发基于血型特征的精准营养方案,例如针对A型血肠道菌群的特异性益生菌制剂。对于个体而言,了解血型特性不应成为健康焦虑的源头,而应作为制定个性化健康管理的科学依据。


