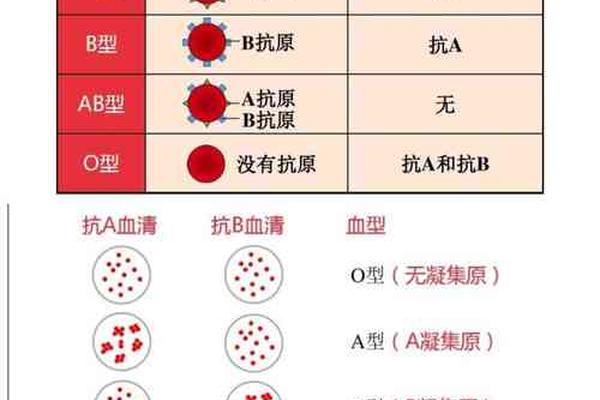
血型系统的核心在于红细胞表面抗原与血浆抗体的特异性关系。在ABO血型系统中,A型血的红细胞携带A抗原,血浆中含有抗B抗体;AB型血的红细胞同时携带A和B抗原,但血浆中无任何抗体。这种生物学特性决定了两种血型的天然互斥性。
从抗原-抗体反应机制来看,当A型血接受AB型血液时,A型血浆中的抗B抗体会与AB型红细胞上的B抗原结合,引发红细胞凝集反应,导致溶血、血栓甚至器官衰竭等致命后果。这一机制在动物实验与临床输血案例中均得到验证,例如2022年剑桥大学的研究显示,跨血型输血必须通过特殊酶处理去除抗原才能实现安全性。

二、输血原则的演变与争议
传统观点曾认为AB型是“万能受血者”,而O型是“万能供血者”,但现代医学已修正了这一认知。根据《临床输血技术规范》,输血需遵循严格的同型原则,仅在紧急情况下允许少量异型输血。例如,A型患者若需输血,首选A型全血,次选A型红细胞与AB型血浆的配合型输注。
争议主要存在于特殊场景下的处理方式。例如,AB型血浆因不含抗A、抗B抗体,理论上可输给A型患者。但2024年最新研究指出,AB型血浆中可能携带其他免疫活性物质,仍存在约3%的迟发性溶血反应风险。即使是成分输血,仍需通过交叉配血试验验证相容性。
三、临床实践中的关键问题
在临床操作层面,A型血接受AB型血液的可行性受到多重限制。红细胞输注绝对禁止,因AB型红细胞携带的B抗原会与A型血浆中的抗B抗体发生剧烈反应。血浆输注需满足特定条件:仅当AB型血浆经抗体效价检测(效价≤1:64)且交叉配血试验阴性时,方可作为A型患者的替代方案。
典型案例显示,2019年宁夏某医院曾为一名B3亚型孕妇实施配合型输血,最终选择O型洗涤红细胞而非AB型血液,原因在于AB型血液的抗原残留风险不可控。这印证了世界卫生组织提出的“最低抗原暴露”原则——优先选择抗原种类更少的血制品以降低免疫风险。
四、科学研究的突破与未来方向
血型转换技术的突破为跨血型输血提供了新思路。2022年剑桥大学团队利用嗜黏蛋白阿克曼菌提取的酶制剂,成功将AB型肾脏转换为O型,移植后3年存活率达97%。这种酶处理技术若应用于血液制品,理论上可实现AB型红细胞向A型的转化,但其工业化生产仍面临酶活性稳定性、成本控制等挑战。
基因编辑技术同样展现潜力。2023年《自然·生物技术》刊文称,CRISPR-Cas9系统可精准敲除造血干细胞中的B抗原基因,使AB型个体产生A型红细胞。该技术在小鼠模型中已实现90%的转化效率,但人体应用仍需解决脱靶效应和审查问题。
现有医学证据表明,A型血不能直接接受AB型全血或红细胞,仅在严格控制的成分输血场景中存在有限的应用空间。输血安全的核心仍在于同型输注原则,异型输血必须建立在完善的实验室检测与风险评估基础上。
未来研究应聚焦两大方向:一是开发更高效的血型转换技术,如纳米酶催化体系或合成生物学路径,实现血型抗原的精准调控;二是建立动态风险评估模型,通过机器学习预测不同血型组合的免疫反应概率,为临床决策提供量化依据。随着技术进步,或许终将打破血型壁垒,但现阶段尊重生物学规律仍是保障输血安全的首要准则。


