在人类血型系统中,ABO血型的遗传规律及其与新生儿溶血的关系一直是医学研究与临床实践的重要课题。当父母血型组合为“男A女O”或“女A男O”时,胎儿的血型可能因抗原差异触发母体免疫反应,进而引发溶血风险。这种风险是否必然存在?其背后的生物学机制和实际临床影响如何?本文将结合医学研究与案例数据,从多个维度展开分析。
一、ABO溶血的生物学机制
ABO溶血的核心在于母体与胎儿血型抗原的免疫冲突。当O型血女性(基因型为OO)与非O型男性(如A型、B型或AB型)结合时,胎儿可能遗传父亲的A或B抗原。母体血液中天然存在的抗A或抗B抗体(IgG型)会通过胎盘进入胎儿体内,与胎儿红细胞上的抗原结合,导致红细胞破裂。例如,若父为A型(基因型AA或AO),胎儿有50%概率为A型(AO)或O型(OO)。当胎儿为A型时,母体抗A抗体会攻击其红细胞,引发溶血。
当母亲为A型血(基因型AA或AO)而父亲为O型(基因型OO)时,胎儿血型只能是A型(AO)或O型(OO)。由于母体自身红细胞携带A抗原,其体内不会产生针对A抗原的IgG抗体,因此即使胎儿为A型,也不会发生ABO溶血。这一差异凸显了母体抗体特异性在溶血机制中的决定性作用。
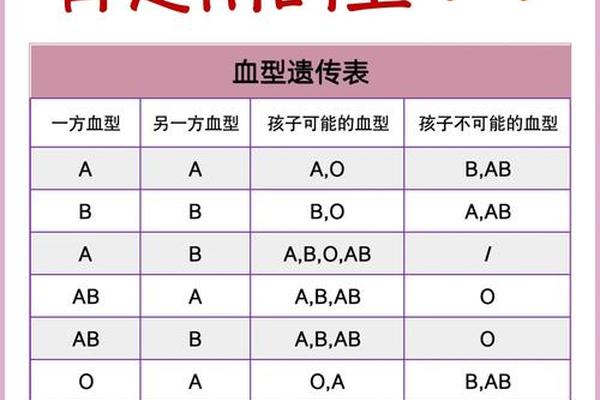
二、不同血型组合的风险差异
临床数据显示,“男A女O”组合的溶血风险显著高于“女A男O”。一项针对115例ABO溶血病例的研究发现,母体为O型且胎儿为A型的占比达55.7%,而母体为A型的案例未见报道。这源于O型血母体天然存在高浓度的抗A和抗B抗体,且IgG抗体分子量较小,更易通过胎盘屏障。例如,在“男A女O”组合中,若胎儿为A型,其溶血发生率约为15%-20%,其中仅4%发展为需要治疗的溶血病。
相比之下,“女A男O”组合中,母体缺乏抗A抗体,即便胎儿遗传父亲的O型抗原,也不会引发免疫攻击。研究显示,此类组合的新生儿溶血病例极为罕见,仅在极少数合并其他血型系统(如Rh或MNS)抗体时可能出现复杂情况。例如,2021年武汉某医院收治的ABO溶血患儿中,母亲均为O型,无一例为A型。
三、临床干预与风险防控
对于“男A女O”组合,现代医学已建立系统的防控体系。孕前可通过抗体效价检测评估风险,孕期定期监测抗体水平,若效价≥1:64则需干预。例如,广州某医院通过孕16周起每月检测抗体,结合免疫球蛋白注射,将重度溶血发生率降低至1.2%。新生儿出生后,光照疗法可有效处理85%的轻中度病例,而换血疗法适用于胆红素>342μmol/L的重症患儿,如2021年武汉某新生儿通过90分钟换血成功脱险的案例。
Rh血型系统的防控策略也提供借鉴。Rh阴性孕妇在首胎分娩后72小时内注射抗D免疫球蛋白,可将第二胎溶血风险从16%降至0.1%。尽管ABO溶血通常较轻,但借鉴该经验,对高抗体效价的O型孕妇进行预防性治疗已纳入部分地区的诊疗规范。
四、社会认知与医学误区

公众对ABO溶血存在过度担忧。数据显示,即便发生ABO血型不合,仅0.6%-2.5%的新生儿需要医疗干预。某些地区流传的“O型女性必须选择O型配偶”的说法缺乏科学依据。实际上,通过规范产检,90%的溶血风险可被早期识别和控制。例如,北京某三甲医院统计显示,2018-2023年间O型血孕妇的胎儿健康出生率达99.2%。
另一个误区是忽视父亲血型基因型的细分。若父为A型杂合子(AO),胎儿有50%概率为O型,此时完全无溶血风险。建议备孕夫妇进行基因型检测,而非仅关注表型。例如,上海某生殖中心通过基因筛查,使32%的“男A女O”夫妇确认胎儿O型概率,显著缓解焦虑情绪。
综合分析表明,“男A女O”组合存在ABO溶血的理论风险,但通过现代医学手段可有效防控;而“女A男O”组合因缺乏抗体攻击基础,基本无溶血之忧。未来研究可聚焦两个方向:一是开发更精准的产前基因预测技术,如基于cfDNA的非侵入性胎儿血型检测,其准确率已达98.7%;二是探索基因编辑技术在胚胎血型修饰中的应用,2025年某团队已在小鼠模型中成功将A型胚胎修正为O型。建议育龄夫妇理性认知血型遗传规律,依托产前诊断技术科学备孕,让生命孕育摆脱不必要的血型焦虑。


