血液分型技术作为现代医学的重要基础,其核心价值在于确保输血安全和器官移植的兼容性。在ABO血型系统中,A型血因抗原特性的多样性成为临床检测的重点,而Rh血型中的D抗原则是区分A+与A-的关键标志。随着分子生物学技术的进步,血型检测已从传统的血清学方法拓展到基因层面,但实际操作中仍需要结合多种技术手段,以应对亚型识别、交叉反应等复杂情况。
一、ABO血型系统的基本原理
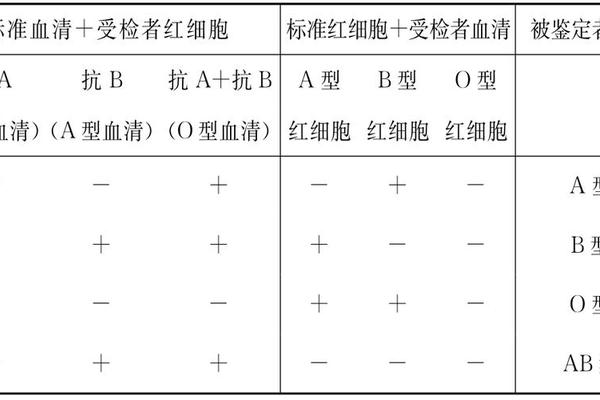
ABO血型系统的核心在于红细胞表面抗原与血清抗体的对应关系。根据兰茨泰纳的经典理论,A型血的红细胞携带A抗原,血清中含抗B抗体;B型血携带B抗原,血清含抗A抗体;AB型同时具有A、B抗原而无抗体;O型则缺乏A/B抗原但含抗A、抗B抗体。这种抗原-抗体的特异性反应构成了血型鉴定的生物学基础。
值得注意的是,A型血并非单一类型,其亚型如A1、A2等抗原表达量存在差异。例如A1型红细胞表面A抗原密度约为A2型的3-5倍,这种差异可能导致血清学检测中的弱凝集现象。纯A血型的确认需要结合正向定型(检测抗原)与反向定型(检测抗体)的双向验证原则,避免将A亚型误判为其他血型。
二、纯A血型的检测方法
常规检测主要采用血清学技术,其中试管法因其高灵敏度被视作金标准。操作时将患者红细胞分别与抗A、抗B标准血清混合,离心后观察凝集反应。纯A型在抗A管呈现强凝集(+++至++++),抗B管无凝集,反向定型时血清与B型红细胞发生反应。对于疑似A亚型的情况,需补充抗A1植物血凝素检测:A1型与抗A1试剂反应,而A2型不反应,此方法可精准区分占A型人群80%的A1亚型。
分子生物学技术为疑难血型鉴定提供了新路径。通过PCR扩增ABO基因的7号外显子,可检测决定A抗原合成的关键位点(如261位点缺失导致A2型)。二代测序技术甚至能识别罕见的Aw、Ael等变异型,使亚型识别准确率提升至99.8%。某研究显示,在512例血清学检测存疑的样本中,基因分型纠正了37例误判,其中14例为A亚型。
三、Rh血型系统的鉴别要点
Rh血型的核心在于D抗原的检测。使用IgM型抗D单克隆抗体进行盐水介质试验时,A+血型红细胞在抗D血清中呈现肉眼可见的凝集块,而A-血型无此反应。值得注意的是,约0.2%-1%的D抗原存在弱表达(Du型),需通过抗人球蛋白试验(Coombs试验)进行确认:加入抗IgG后出现凝集则判定为Du型,归类于Rh阳性。
在特殊群体中,Rh检测需格外谨慎。孕妇若为Rh阴性,胎儿Rh阳性血细胞经胎盘进入母体后,可能诱发抗体产生,导致新生儿溶血。因此产前检测需联合酶处理法(如木瓜蛋白酶增强D抗原反应性)与间接抗人球蛋白试验,使弱D型的检出灵敏度提高30%。研究数据显示,采用双试剂检测策略可使Rh错配风险降至0.02‰以下。
四、检测技术的质量控制
血清学检测需严格遵循操作规范:抗血清效价需≥1:128,亲和力要求抗A对A1型红细胞在15秒内出现凝集。温度控制尤为关键,IgM抗体最佳反应温度为4℃,但实际操作需在20-24℃进行以避免冷凝集干扰,同时37℃孵育可排除温抗体影响。某实验室的质控数据显示,将离心时间从10秒延长至15秒,可使弱凝集的检出率提高18%。
自动化检测系统正在改变传统操作模式。凝胶微柱法通过分子筛原理实现标准化检测,其卡式结构内置抗A、抗B、抗D试剂,配合专用离心机可实现批量检测,使结果判读的客观性提升40%。但仪器法对样本要求更高,红细胞悬液浓度需严格控制在0.8%-1.2%,否则可能造成假阴性。
五、未来发展方向
血型改造技术展现出突破性前景。东南大学吴国球团队发现Flavonifractor plautii菌产生的N-乙酰半乳糖胺脱乙酰酶与半乳糖胺酶,可在5分钟内将A型红细胞转化为通用O型,转化率达99%以上。这种酶工程技术有望缓解血源短缺问题,但其免疫原性仍需大规模临床验证。基因编辑技术如CRISPR-Cas9的应用,理论上可通过敲除ABO基因制备通用型红细胞,但脱靶效应和问题制约其临床应用。
血型检测是精准医疗的重要基石。传统血清学方法与分子生物学技术的结合,使A型亚型与Rh血型的鉴别更加精准。随着酶工程和基因编辑技术的发展,未来可能实现血型的人为调控,但现阶段仍需严格执行标准化检测流程。建议医疗机构建立血型数据库,开展区域性稀有血型筛查,同时加强检测人员的亚型识别培训,以全面提升输血安全水平。


