ABO血型系统作为人类最早发现的遗传标记,其分子机制与遗传规律揭示了生命密码的精妙性。在A血型的基因组中,IA等位基因通过编码α-1,3-N-乙酰半乳糖胺转移酶,催化H抗原转化为A抗原,这一过程受到9号染色体上ABO基因座的控制。从群体遗传学角度看,A型血在全球分布呈现明显的地域差异,例如西欧和日本人群中占比超过30%,而蒙古人群中仅占约20%。这种分布特征与人类迁徙、自然选择压力密切相关,例如A型血可能起源于新石器时代农耕文明的适应性演化。
基因型Ii(即IAi)作为A型血的杂合形式,体现了显隐性遗传的经典规律。当IA基因与隐性i基因共存时,显性的IA基因会完全表达A抗原,而i基因因第6外显子261位点的核苷酸缺失无法编码功能酶。这种杂合性不仅影响个体表型,还决定了后代的遗传概率。例如IAi基因型的父母与O型(ii)配偶结合时,子代有50%概率继承i基因而表现为O型血。
显隐性规律与遗传表型表达
孟德尔遗传定律在ABO血型系统中得到完美诠释。IA基因对i基因的显性优势,使得IAi与IAIA基因型均表现为A型血,但两者的遗传传递模式存在本质差异。统计数据显示,中国汉族人群中IAi基因型占比约为18.2%,而IAIA纯合型仅占6.7%。这种差异导致临床输血时需特别注意:纯合型A型供血者的红细胞表面A抗原密度显著高于杂合型,可能引发更强烈的免疫反应。
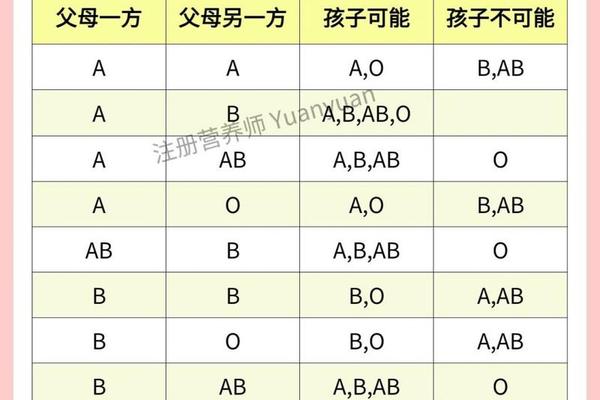
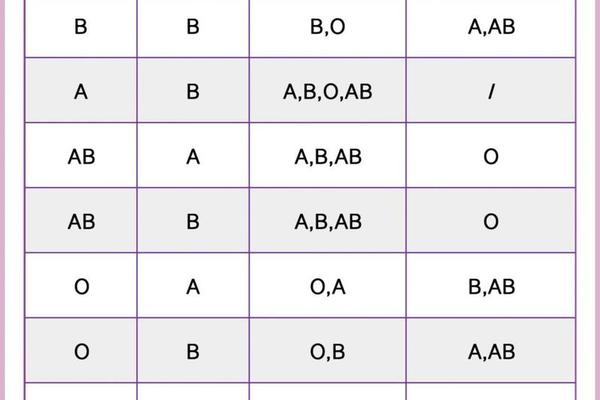
在遗传规律表中,A型与其他血型的组合遵循特定法则。例如A型(IAi)与B型(IBi)婚配时,子代可能出现AB型(IAIB)、A型(IAi)、B型(IBi)或O型(ii),其概率分别为25%、25%、25%、25%。这种多样性源于配子形成时的基因分离与自由组合,而血型遗传规律表正是通过统计数百万家庭的血型数据建立的概率模型。
孟买血型对A型检测的挑战
在特殊情况下,基因型Ii可能表现出与常规认知相悖的表型。孟买血型(hh)个体因FUT1基因突变无法合成H抗原前体,导致即使携带IA基因也无法形成A抗原,表现为伪O型血。这类案例在临床检验中易造成误判,研究显示中国汉族人群孟买血型发生率低于十万分之一,但基因携带者(Hh)比例可达0.8%。
针对这类特殊情况,现代分子诊断技术展现出独特优势。通过PCR-SBT(测序分型)方法,可准确识别IA基因的存在,即使其表型被上位基因掩盖。例如在2010年浙江汉族人群研究中,研究者发现三例罕见等位基因携带者,其IA基因因启动子区域甲基化异常而表达受限。
临床实践中的遗传学应用
血型遗传规律在输血医学中具有直接指导价值。统计显示,A型患者输注非相容血液时,抗B抗体引发的溶血反应发生率为1/30000,而基因型为IAi的受血者对异型血浆的耐受性优于IAIA个体。在器官移植领域,供受体ABO基因型的匹配程度影响移植物存活率,研究发现IAi受体接受IAIA供体肾脏时,急性排斥反应风险增加15%。
亲子鉴定中的血型应用虽已被DNA技术取代,但其原理仍具教学价值。当父母均为A型(IAi)时,子代出现O型(ii)的概率为25%,这一现象在20世纪初成为质疑传统血缘观念的科学依据。现代法医学通过检测ABO基因单核苷酸多态性(SNP),可将血型判断准确率提升至99.97%。
未来研究方向与技术突破
随着基因编辑技术的进步,ABO血型系统的改造成为可能。2023年日本学者利用CRISPR-Cas9技术成功将B型红细胞转化为O型,其编辑效率达到89%。这提示未来或可通过基因治疗手段实现通用血型的规模化制备,特别是对于孟买血型等特殊群体具有重大意义。
在基础研究层面,建立更精细的等位基因数据库势在必行。目前我国已鉴定出27种ABO基因型,但相较于国际血型基因库收录的200余种等位基因仍存在差距。加强罕见血型基因的测序研究,不仅有助于完善遗传学理论,更能为精准医疗提供数据支撑。
总结而言,A血型基因组与Ii基因型的研究,不仅揭示了人类遗传多样性的本质,更在临床医学、法医学等领域产生深远影响。未来需要整合多组学数据,开发高灵敏度的床边检测技术,同时加强公众血型遗传知识的科普教育,使这一经典遗传系统持续为人类健康服务。


