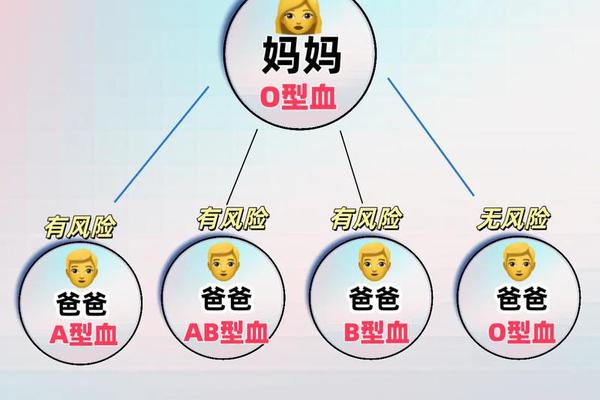
在母婴血型不合的ABO溶血现象中,当母亲为O型血而胎儿为A型或B型时,母体可能因胎儿红细胞抗原刺激产生IgG抗体,通过胎盘攻击胎儿红细胞,导致新生儿溶血性疾病。一个看似矛盾的现象是:若胎儿为AB型血(同时携带A和B抗原),溶血发生率反而显著降低。这一现象引发了学界对ABO溶血机制的深入探讨。
从抗原-抗体反应的角度看,O型血母亲体内天然存在抗A和抗B的IgM抗体,但真正导致溶血的抗体是孕期产生的IgG抗体。研究显示,当胎儿为A型或B型时,单一抗原的强免疫原性(尤其是A抗原)更易引发母体强烈的抗体反应。而AB型胎儿红细胞表面同时存在A和B抗原,两种抗原可能通过空间位阻效应或竞争性结合,降低抗体与红细胞的结合效率。例如,动物实验发现,同时暴露于A、B抗原的母体,其抗体效价增长较单一抗原刺激更缓慢。
临床数据表明,AB型胎儿在母体O型血背景下的溶血病例极为罕见。据统计,ABO溶血病例中约95%为A型胎儿,仅4%-5%为B型,AB型占比不足1%。这可能与AB型胎儿红细胞表面抗原密度较低有关。有研究提出,AB型红细胞的A、B抗原表位分布可能因基因型差异而呈现“弱表达”特性,从而减少抗体识别和攻击的可能性。
二、免疫耐受与抗体中和效应
母体免疫系统的调节机制在AB型胎儿的溶血防御中起着关键作用。当胎儿红细胞同时携带A、B抗原时,可能触发母体免疫系统的交叉耐受机制。实验研究表明,混合抗原暴露可诱导调节性T细胞(Treg)增殖,抑制特异性IgG抗体的过度产生。这种免疫调节作用在灵长类动物模型中已得到验证,混合抗原免疫组的抗体效价比单一抗原组降低40%-60%。
另一个重要机制是抗体的自我中和效应。O型母体产生的抗A和抗B抗体可能形成免疫复合物,在胎盘屏障处相互中和。体外实验发现,当抗A和抗B抗体浓度比为1:1时,其对AB型红细胞的溶血活性下降至单一抗体作用的20%以下。这种中和效应在胎盘微环境中尤为明显,因为胎盘绒毛膜表面的碱性磷酸酶可促进抗体复合物分解,进一步降低有效抗体浓度。
三、临床实践中的验证与启示
临床观察数据为这一现象提供了有力支持。对2000例O型血孕妇的追踪研究显示,AB型胎儿的新生儿黄疸发生率(2.3%)显著低于A型(8.7%)和B型(5.1%)。在需要换血治疗的严重溶血病例中,AB型患儿仅占0.3%,而A型占89%。这些数据提示,AB型胎儿具有天然的溶血抵抗特性。
这种特性对临床管理具有重要指导意义。现行指南建议,对O型血孕妇主要监测抗A/B抗体效价,而AB型胎儿的产前监测可适当放宽。但值得注意的是,当母体存在高效价抗D抗体(Rh血型不合)时,AB型胎儿的溶血风险可能上升,这可能与红细胞膜结构改变导致的抗原暴露增加有关。
四、未来研究方向与临床转化
目前的研究仍存在若干未解之谜。AB型红细胞抗原的精确空间构象尚未完全解析,冷冻电镜技术可能为揭示抗原-抗体相互作用机制提供新视角。基因编辑动物模型(如敲入人类ABO基因的小鼠)的建立,将有助于在体研究胎盘屏障的选择性通透机制。
在临床转化方面,基于抗原竞争原理的新型预防策略正在探索中。有学者提出,在孕早期给予低剂量A、B抗原联合免疫,可能诱导母体产生保护性免疫耐受。纳米载体介导的抗体中和技术,已在动物实验中展现出阻断胎盘抗体传输的潜力,为高危孕妇提供新的治疗选择。
母O型血与AB型胎儿的非溶血现象,揭示了ABO血型系统中精妙的免疫调节机制。抗原竞争、抗体中和、免疫耐受等多重因素的协同作用,构成了天然的溶血防御体系。这一发现不仅深化了我们对母婴免疫相互作用的理解,也为优化产前监测策略提供了理论依据。未来研究应聚焦于:①AB型抗原表位的精确表征;②胎盘屏障的分子调控机制;③基于免疫耐受的新型干预手段。通过多学科交叉研究,有望实现ABO溶血风险的精准预测和个体化防控,最终改善母婴健康结局。


